SCDM Annual Conference 2017 参加報告

9月24日-27日にアメリカフロリダ州のオーランドで開催された Society for Clinical Data Management(SCDM)の Annual Conference の参加報告です。
9月前半、2つの大きなハリケーンがフロリダ州を襲いましたが、会場であるオーランドには大きな被害もなく無事開催されました。
24日には、Pre-Conference として、データマネジャー(DM)向けの Risk-based Monitoring(RBM)と FDA submission の workshop が開催されました。RBMのworkshopでは、RBMに関する基本的な用語やアプローチの整理が中心でしたが、Quality Tolerance Limits(QTL)など、まだ十分に認知されていないコンセプトについての解説やディスカッションもあり、またICH-E6 R2の最終合意(Step4)後の製薬企業やCROの対応状況について、海外の実際の状況についても知ることもできて参考になりました。
プログラム本体は、2日半の日程で開催され、トピックとしてはRBMやeSource関連のセッションが多い印象を受けました。RBMについては、昨年度までは、方法論の整理や動向についての総論的な内容が主でしたが、今年は実際にシステムを活用したセントラルモニタリングの事例やAIを活用した事例の発表もあり、RBMが現場でも実践され始めていることを実感した年でした。eSource以外には、ePROのセッションもあり、こちらは海外でもだいぶ実際の臨床試験で活用されているようでした。eConsentの活用は、今後のホットな話題になりそうですが、技術的にはすでに実践できるレベルにきており、展示ブースではeConsentのシステムを宣伝しているベンダーも多く出展していました。
日本からの発表では、初日最後のRegulatory session において、パネリストとしてPMDAから2名が登壇され、PMDAの査察の実施状況やeCTDやCDISCによる試験データの受付についての紹介があり、さらに会場とのデスカッションもありました。一般演題としては、最終日のアカデミアのセッションにおいて、当分野の山口 拓洋 教授より、日本のアカデミアにおけるデータマネジャーの現状、および、2012年から東北大学で実施している臨床研究従事者の専門家のための大学院プログラムの紹介をさせていただきました。米国においても、Duke大学やCincinnati大学などでは、DM向けのプログラムがあり、最近ではアーカンソー州にあるUAMSメディカルセンターが、Biomedical informatics専攻として、大学院プログラムを開始しています。
ポスターセッションは、60演題近くの申し込みがあったようですが、最終的には7演題のみが採択され、そのうち4演題が日本からの応募演題でした。日本からの演題が多く採択された事自体ももちろん誇らしいですが、さらにポスターセッションでの発表と選考委員による審査を経て、最優秀賞(1st Prize)をエイツーヘルスケア株式会社の近藤氏が、優秀賞(3rd Prize)を当分野の邱 士韡 助教が受賞しました。発表内容は、それぞれRBMとCDISCの教育プログラムに関するもので、当分野が、東北大学病院 臨床試験データセンターや東京大学大学院 臨床試験データ管理学講座とともに5年程前から主催してきた産学連携の勉強会からの成果物であり、それがCDMの国際学会で認められたことは非常に名誉なことでした。今後は、国内に留まらず、国際的にも教育や研究について貢献できるような活動に発展させていければと思います。
今回のSCDMでは、要所要所で日本の活動を世界のCDMコミュニティーに向けて発信することができたように思えます。当講座としては、数年前からSCDMのAcademic Task Forceに参加し、国内の活動の発信と海外との交流を促進するように働きかけておりましたが、SCDMの日本支部の話も少しずつですが前進しており、SCDMの理事メンバーを含めたSteering committeeを立ち上げ、設立に向けて調整をしている段階です。進捗については、ホームページを通して随時ご報告させていただきます。
来年は、アメリカ西海岸側での開催の年、ワシントン州シアトルにおいて、9月23日から26日まで開催予定です。

■写真1■ 初日のRegulatory session
右からKassa Ayalew氏(FDA)、安藤 友紀 氏(PMDA)、森川 華子 氏(PMDA)

■写真2■ ポスター発表の様子1
筆頭発表者:高田 宗典 先生(東大附属病院 臨床研究支援センター)
『Construction of Complex Database Integrating Data from ePRO for Intractable Disease』
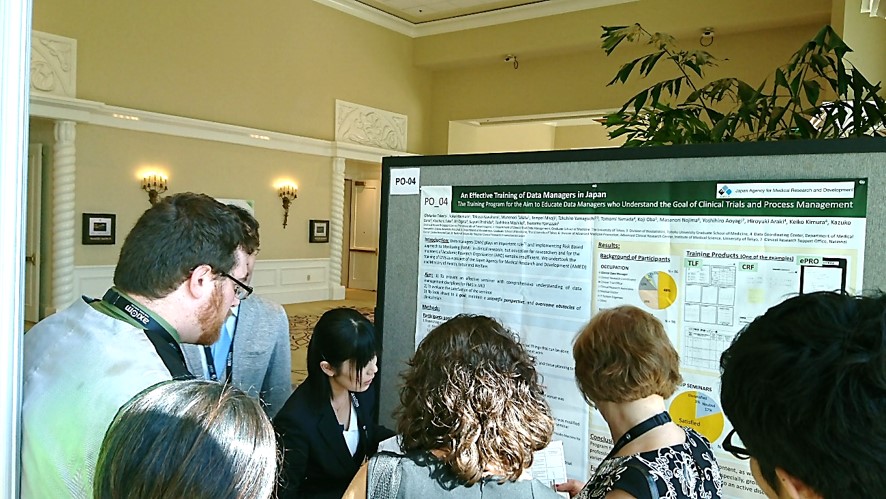
■写真3■ ポスター発表+審査の様子
筆頭発表者:竹田 万里子 先生(東大附属病院 臨床研究支援センター)
『An Effective Training of Data Managers in Japan. The Training Program for the Aim to Educate Data Managers who Understand the Goal of Clinical Trials and Process Management』

■写真4■ ポスター演題優秀賞受賞式
筆頭発表者:邱 士韡 助教
東北大学大学院医学系研究科 医学統計学分野 / 東北大学病院 臨床試験データセンター
『After understanding the CDISC standards, what is the next step? -Practical Training Program for Data Manager-』

■写真5■ ポスター演題最優秀賞受賞式
筆頭発表者:近藤 秀宣 氏
エイツーヘルスケア株式会社 開発戦略本部 セントラルモニタリング部
『Survey of organization-specific and role-specific training needs for RBM related tasks in Japan』

■写真6■ 口頭発表
セッション<Professional Development and Graduate Degree Programs for CDM>
発表者:山口 拓洋 教授
東北大学大学院医学系研究科 医学統計学分野・東北大学病院 臨床試験データセンター
『Professional Training Course for Clinical Data Management in Tohoku University』

■写真7■
日本からの参加メンバーの集合写真。数年前までは毎年5,6人でしたが、本年は、製薬企業・CRO・アカデミア合わせて15名が参加しました。









